JAKARTA, studyinca.ac.id – Dalam dunia kimia, setiap zat terbentuk karena adanya gaya tarik antar atom. Salah satu bentuk gaya tarik yang paling mendasar adalah ikatan ion. Istilah ini merujuk pada proses pembentukan senyawa akibat adanya transfer elektron antara atom logam dan non-logam.
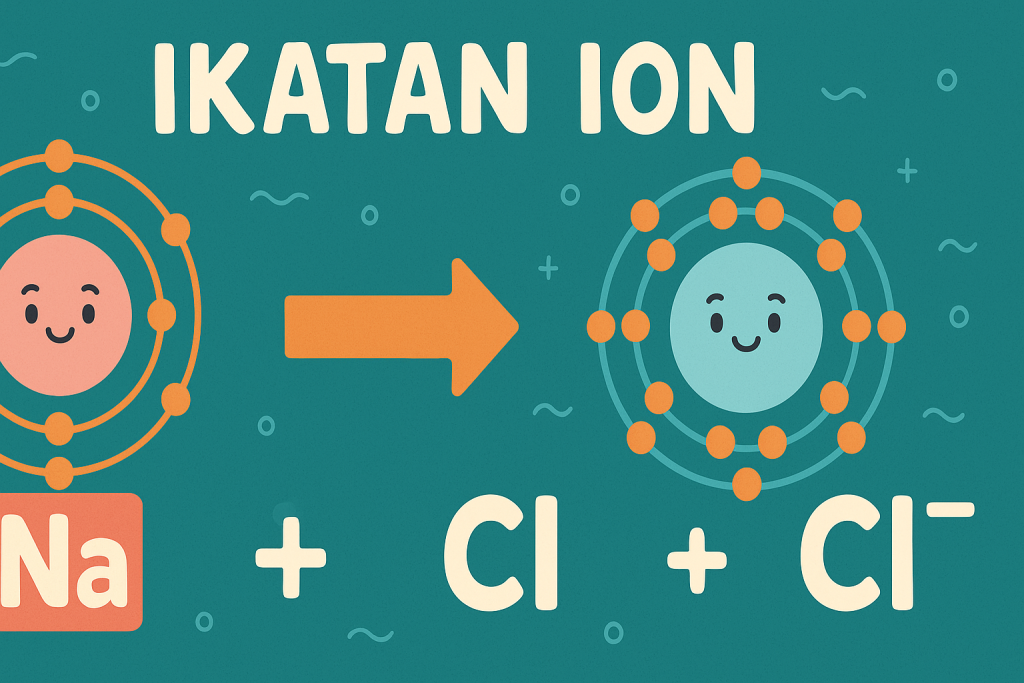
Ikatan ion terjadi ketika satu atom melepaskan elektron, sementara atom lain menerima elektron tersebut. Hasilnya, terbentuk dua ion bermuatan berlawanan — kation (positif) dan anion (negatif) — yang saling tarik-menarik membentuk struktur stabil.
Contoh paling sederhana dari ikatan ion dapat ditemukan pada natrium klorida (NaCl), yaitu garam dapur. Di sini, atom natrium (Na) melepaskan satu elektron kepada atom klor (Cl), membentuk senyawa padat kristalin yang kuat dan stabil.
Proses Terbentuknya Ikatan Ion
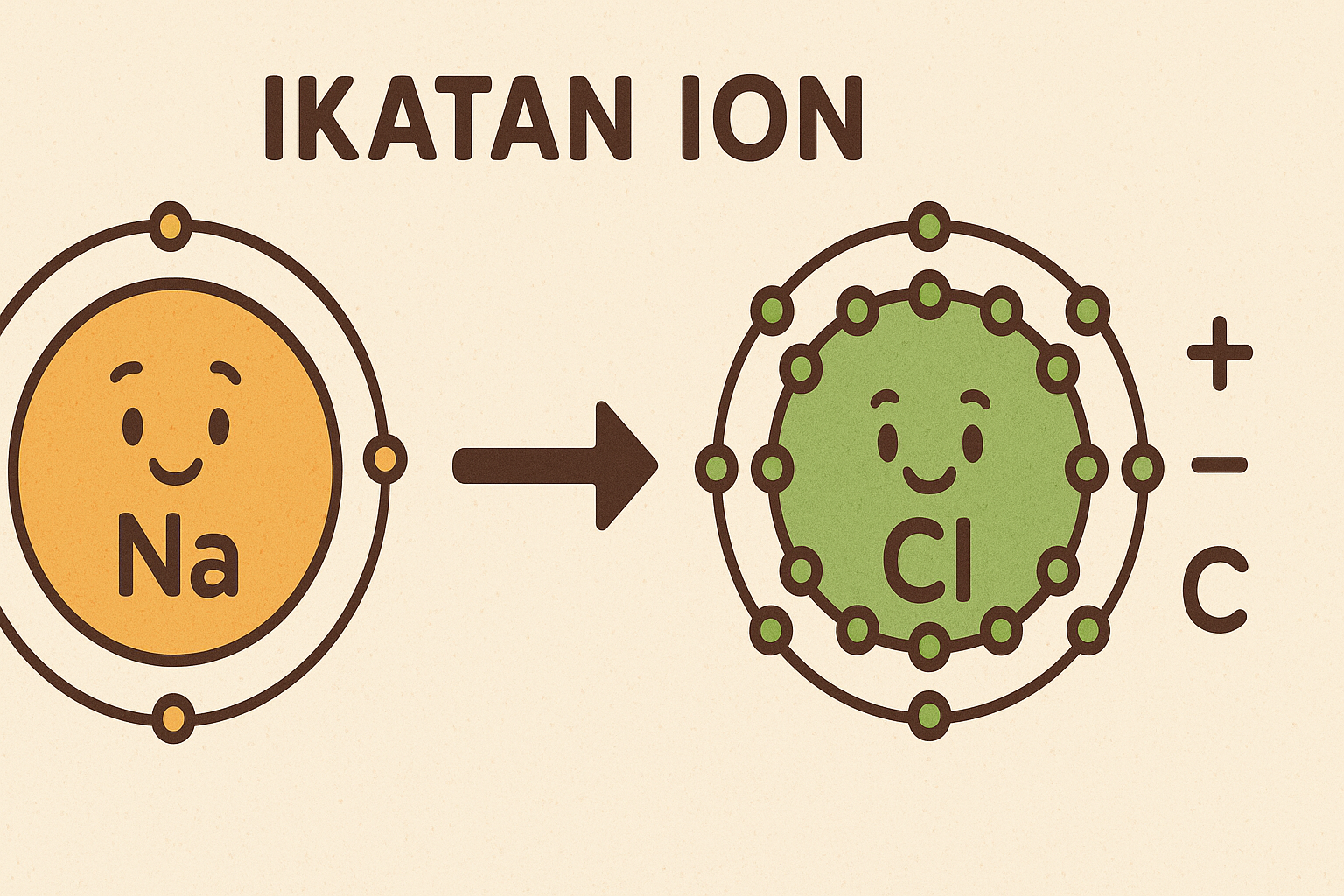
Agar lebih memahami konsepnya, mari kita lihat langkah-langkah pembentukan ikatan ion secara sistematis:
-
Transfer Elektron
Atom logam cenderung melepaskan elektron karena memiliki energi ionisasi rendah. Sebaliknya, non-logam memiliki afinitas elektron tinggi dan cenderung menerima elektron.Contoh:
-
Na (logam) → Na⁺ + e⁻
-
Cl (non-logam) + e⁻ → Cl⁻
Ketika kedua proses ini terjadi bersamaan, terbentuklah senyawa NaCl yang stabil.
-
-
Pembentukan Gaya Tarik Elektrostatis
Setelah transfer elektron, terbentuk ion bermuatan positif dan negatif. Gaya tarik elektrostatik antara kedua ion inilah yang disebut ikatan ion. -
Struktur Kristal Padat
Ion-ion tersusun dalam pola tiga dimensi yang teratur, menciptakan struktur kristal yang kuat. Pola ini membuat senyawa ionik memiliki titik leleh tinggi dan tidak mudah hancur. -
Keseimbangan Energi
Saat ikatan terbentuk, energi dilepaskan. Proses ini disebut energi kisi (lattice energy), yaitu ukuran kekuatan ikatan antar ion dalam struktur kristalnya.
Ciri-Ciri Senyawa dengan Ikatan Ion
Senyawa yang memiliki ikatan ion menunjukkan karakteristik khas yang membedakannya dari jenis ikatan lainnya seperti ikatan kovalen atau logam. Berikut ciri-ciri utamanya:
-
Berwujud Padat Kristalin
Sebagian besar senyawa ionik seperti garam dapur, magnesium oksida, dan kalsium klorida berbentuk padatan keras dengan permukaan kristal. -
Memiliki Titik Leleh dan Didih Tinggi
Gaya tarik antara ion positif dan negatif sangat kuat, sehingga diperlukan energi besar untuk memisahkan mereka. -
Larut dalam Air
Senyawa ionik umumnya larut dalam air karena molekul air bersifat polar dan mampu memisahkan ion-ion di dalamnya. -
Dapat Menghantarkan Listrik dalam Larutan atau Lelehan
Ion bebas yang terbentuk dalam larutan memungkinkan aliran listrik. Namun, dalam bentuk padat, senyawa ionik tidak menghantarkan listrik karena ion-ionnya terikat kuat. -
Rapuh Saat Ditekan
Ketika gaya tekan diberikan, ion dengan muatan sejenis bisa saling berdekatan dan tolak-menolak, menyebabkan senyawa mudah pecah.
Contoh Senyawa yang Memiliki Ikatan Ion
Beberapa senyawa umum yang terbentuk melalui ikatan ion antara lain:
| Senyawa | Unsur Pembentuk | Nama Kimia | Keterangan |
|---|---|---|---|
| NaCl | Natrium dan Klor | Natrium Klorida | Garam dapur yang digunakan sehari-hari |
| MgO | Magnesium dan Oksigen | Magnesium Oksida | Digunakan dalam bahan tahan panas |
| CaCl₂ | Kalsium dan Klor | Kalsium Klorida | Menyerap kelembapan dan digunakan dalam industri |
| KBr | Kalium dan Brom | Kalium Bromida | Digunakan dalam fotografi dan obat-obatan |
| LiF | Litium dan Fluor | Litium Fluorida | Digunakan dalam lensa optik dan baterai |
Contoh-contoh di atas menunjukkan betapa luas peran ikatan ion dalam berbagai aspek kehidupan manusia, mulai dari dapur hingga industri modern.
Perbedaan Ikatan Ion dan Ikatan Kovalen
| Aspek | Ikatan Ion | Ikatan Kovalen |
|---|---|---|
| Cara Terbentuk | Transfer elektron antar atom | Berbagi pasangan elektron |
| Jenis Unsur | Logam dan non-logam | Dua non-logam |
| Sifat Fisik | Padat, titik leleh tinggi | Bisa padat, cair, atau gas |
| Daya Hantar Listrik | Menghantarkan listrik dalam larutan | Umumnya tidak menghantarkan listrik |
| Contoh | NaCl, MgO, KBr | H₂O, CO₂, CH₄ |
Perbedaan ini menegaskan bahwa ikatan ion cenderung menghasilkan senyawa stabil dan keras, sedangkan ikatan kovalen lebih fleksibel dan sering ditemukan pada molekul organik.
Peran IkatanIon dalam Kehidupan Sehari-Hari
Ikatan ion tidak hanya penting dalam teori kimia, tetapi juga memiliki peranan nyata dalam kehidupan manusia:
-
Keseimbangan Elektrolit dalam Tubuh
Senyawa seperti NaCl dan KCl membantu menjaga tekanan osmotik dan fungsi saraf manusia. -
Industri Farmasi dan Makanan
Garam dan senyawa ionik lainnya digunakan dalam obat-obatan, pengawet, dan bahan tambahan makanan. -
Teknologi Baterai dan Energi
Ion logam seperti litium dalam baterai modern bekerja berdasarkan prinsip perpindahan ion untuk menghasilkan energi listrik. -
Bahan Bangunan dan Keramik
Senyawa seperti kalsium oksida dan magnesium oksida digunakan untuk membuat semen, kaca, dan bahan tahan panas.
Dengan kata lain, konsep sederhana tentang ikatan ion ternyata menjadi dasar bagi banyak teknologi dan proses biologis yang menopang kehidupan manusia modern.
Kesimpulan
Ikatan ion adalah hasil transfer elektron antara atom logam dan non-logam, menghasilkan gaya tarik elektrostatik yang kuat antara kation dan anion. Senyawa yang terbentuk umumnya padat, memiliki titik leleh tinggi, dan larut dalam air.
Lebih dari sekadar konsep kimia, ikatan ion memiliki dampak luas — dari pembentukan garam dapur hingga teknologi energi modern. Memahami cara kerja dan sifatnya membantu kita mengerti bagaimana alam bekerja di tingkat paling dasar.
Dengan pemahaman yang baik tentang ikatan ion, kita dapat melihat hubungan yang indah antara struktur atom, reaksi kimia, dan kehidupan nyata yang bergantung padanya.
Baca juga konten dengan artikel terkait tentang: Pengetahuan
Baca juga artikel lainnya: Pecahan Campuran: Konsep dan Cara Menghitung